第一部分:疫苗对新冠变异株有效性评价
1、康复/疫苗产生的抗体对变异株的作用普通下降
康复12个月后的康复者血清针对delta毒株的抗体效价相比较alpha低4倍。2剂辉瑞疫苗针对delta毒株的中和效价比alpha低3~5倍[4]。变异毒株可能对一些抗体疗法产生不良影响。
余宏杰教授课题组在CID上发表的meta分析研究显示,既往感染原型株个体的血清针对Beta变异株的中和抗体水平下降4.1倍,针对Gamma变异株的中和抗体水平下降了1.8倍,针对Delta变异株的中和抗体水平下降了3.2倍,针对Alpha变异株的中和抗体水平仅有略微下降(1.4倍,1.2-1.6)。
针对不同研发平台新冠疫苗所诱导的免疫应答,Beta变异株的免疫逃逸最为显著。在活病毒中和实验中,非复制性载体疫苗接种者的血清针对Beta变异株的中和抗体较原型株降低了7.1倍,mRNA疫苗接种者的血清中和抗体较原型株降低了4.1倍,蛋白亚单位疫苗接种者的血清中和抗体较原型株降低了2.5倍。此外,若以携带D614G突变位点的毒株为参考,灭活疫苗接种者的血清对Delta变异株的中和抗体下降了2.4倍,非复制性载体疫苗和mRNA疫苗的接种者血清对Delta变异株的中和抗体则分别下降1.8倍和1.6倍。
2、疫苗对变异毒株的有效性(更新到8.16日)
美国CDC的数据显示,接种疫苗可以使感染风险下降8倍,住院和死亡风险下降25倍。
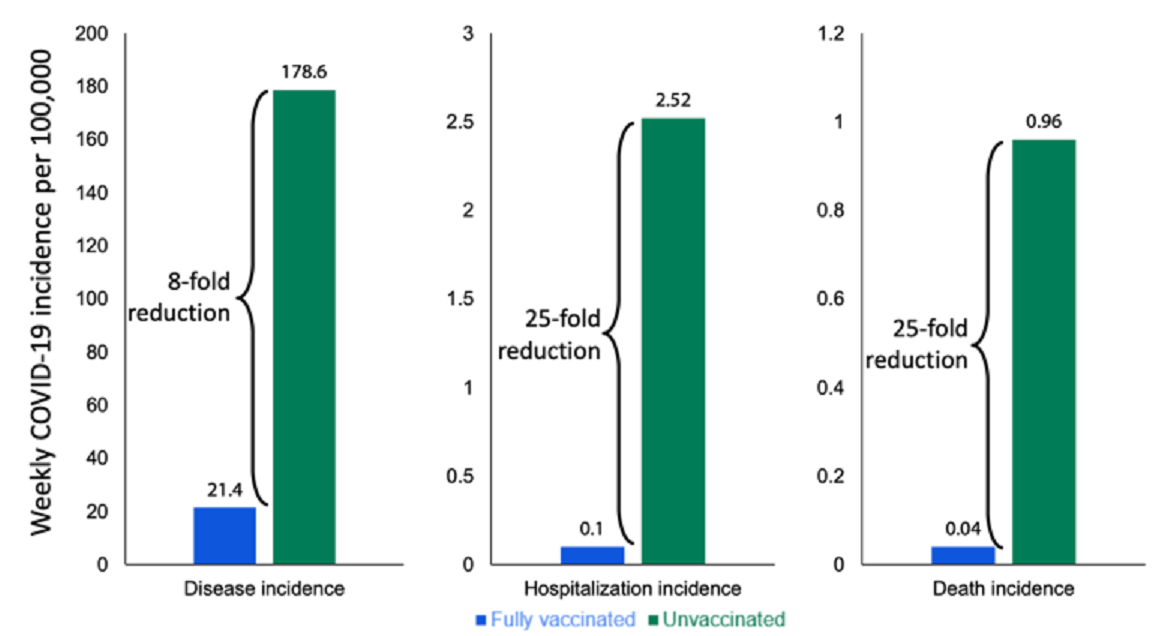
辉瑞mRNA疫苗的有效性
英国公共卫生局的结果显示,对于有症状的感染,两剂辉瑞疫苗对Delta毒株和Alpha毒株的有效性分别是88%和93%,两剂阿斯利康疫苗对这两种毒株的有效性分别是60和66%。但接种疫苗依然可以有效避免重症,辉瑞疫苗接种两剂后可将感染Delta毒株后住院的风险降低96%;阿斯利康疫苗接种两剂后可将住院风险降低92%。加拿大的结果显示,辉瑞疫苗对delta毒株的保护率为87%,对alpha毒株的保护率是89%。
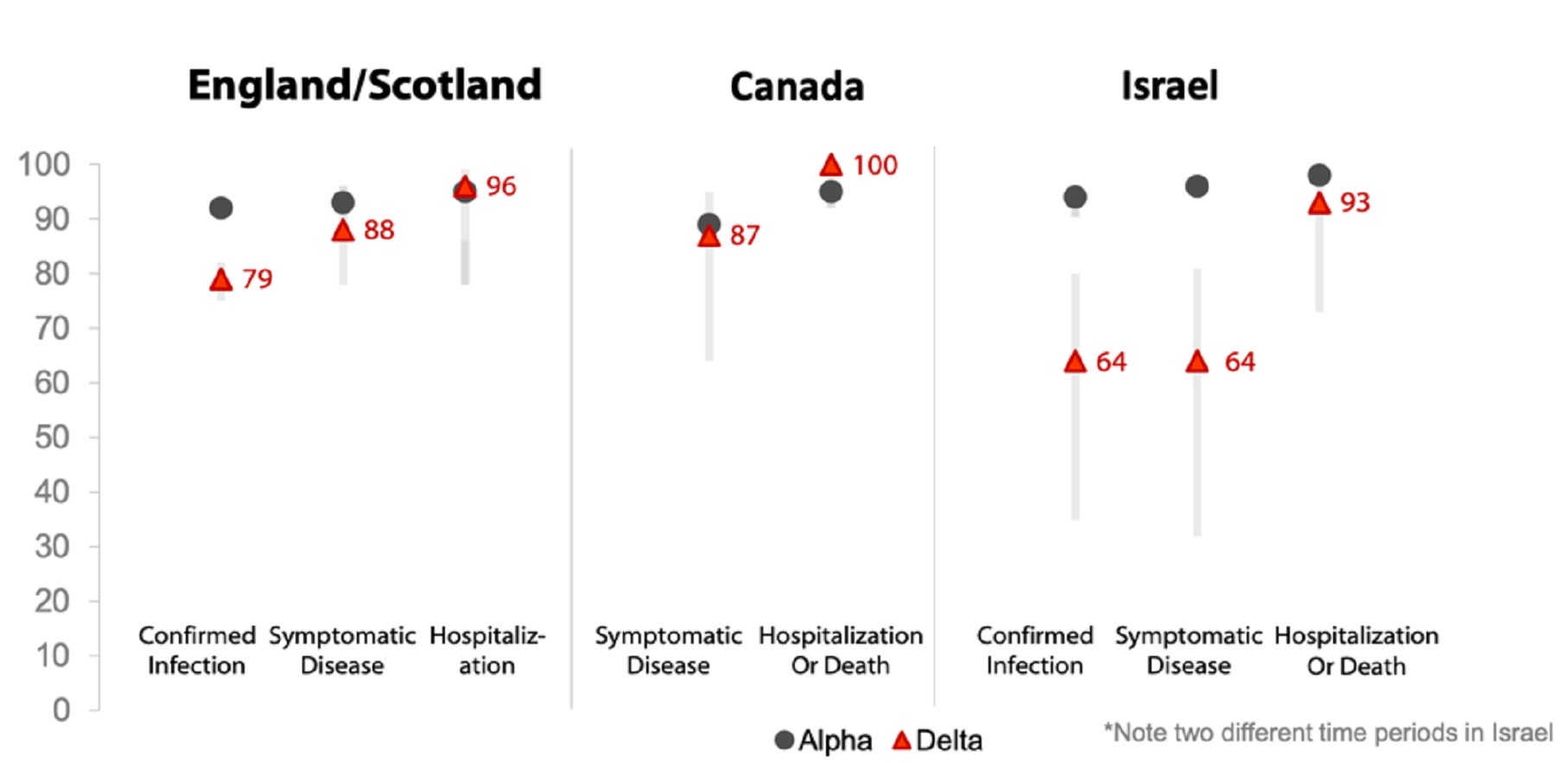
辉瑞mRNA疫苗对Alpha和Delta变异株的有效性
但以色列卫生部门5月份的数据显示,辉瑞疫苗对delta毒株的保护率只有64%,7月以色列的最新数据显示,辉瑞/BioNTech的疫苗防感染的保护率降至39%。不过,以色列尚未公布这些结果背后的详细数据。当地一些专家认为,目前的统计结果可能因为种种原因并不准确,包括感染人数仍然过少、未接种人群感染率不准等但具体的研究数据还未公开,研究纳入的患者数目也较少。
在免疫抑制的人群中,疫苗的保护作用降低,接种两剂mRNA疫苗7-27天后,预防感染的有效性降低到71%,预防出现症状的感染的有效性降低到75%,接种两剂mRNA疫苗14天后,预防住院的有效性降低到59%
国产科兴疫苗在土耳其临床实验的保护率达到了83.5%。在智利的临床实验中,针对新冠的整体有效性达到了65.9%,防住院有效性87.5%,降低进入重症监护室风险90.3%,降低死亡风险86.3%,但对变异毒株的预防效果未做研究。
尽管辉瑞和moderna的mRNA疫苗在表现出较好的效果,但开发中第三种mRNA疫苗效果不尽如意。6月,德国CureVac疫苗公司公布了其在40,000人中的三期试验结果,显示该公司开发的mRNA疫苗保护率仅为47%。CureVac开发的mRNA成本更低,可以在常规冰箱储存更长时间,被认为是可以大量供应发展中国家。这说明mRNA疫苗的开发并不是水到渠成。
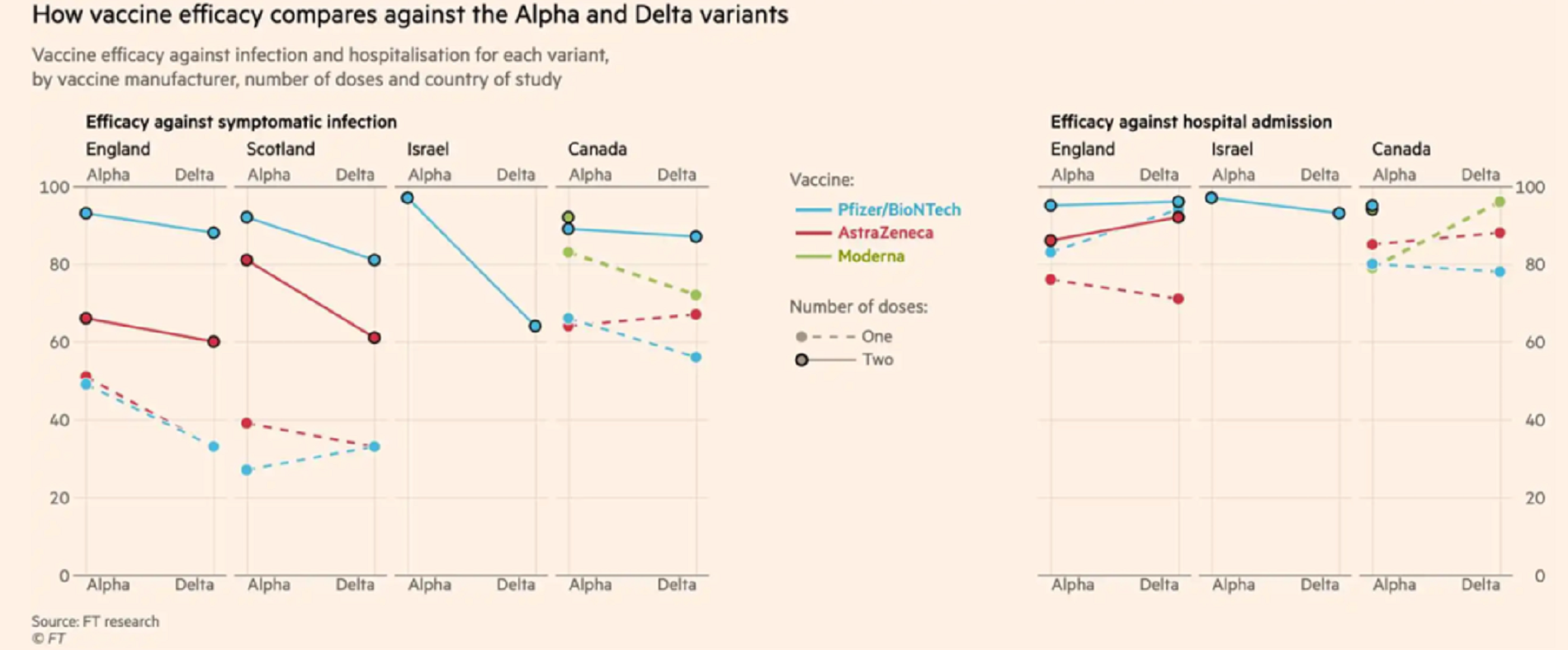
疫苗对各种变异毒株的有效性
3、混合接种和第三针
混合接种:英国和西班牙的研究显示,第一剂腺病毒载体疫苗+第二剂mRNA疫苗的人群,中和抗体水平高于接种两剂腺病毒载体疫苗的人群,而且不良反应程度更低,混合接种似乎具备更高度的安全性和有效性 。加拿大在6月宣布允许第一剂接种腺病毒载体疫苗的人群第二剂接种mRNA疫苗。
加强针/第三针:小样本(<100人)人群和器官移植的患者中实验显示,第三针mRNA疫苗可以加强对疫苗反应弱的人群体液免疫反应,在部分人群中产生的比两针疫苗更高的抗体滴度。基于此,以色列在考虑为高危职业人群补种第三针疫苗。但第三针疫苗是否可以提高对病毒的保护力目前并没有证据,美国CDC和FDA也认为打第三针疫苗的时机并不成熟。但8月德国开始为12-17岁打加强针,以抵抗Delta毒株的感染。
科兴的研究显示,打完两针剂次的志愿者,在隔三个月或六个月后接种第三针,抗体载量可以迅速上升10倍,在老年人中抗体上升的程度更高。
4、接种疫苗后的突破病例
尽管接种疫苗可以有效的防止新冠感染,但由于目前大部分国家疫苗接种率并未达到群体免疫的阈值,加之部分变异毒株传播性的提高,使实现群体免疫的难度再次加大。在当年欧美感染基数仍然高企的情况下,接种疫苗的人群出现感染,及突破病例的出现是理疗之中的事情。
Delta 毒株突破病例的病毒载量是alpha毒株患者的10倍左右,显示突破病例可能和未免疫病例具有相当的传染性。
在美国麻省州469名聚会相关的covid-19患者中,有346(74%)人是接种两针mRNA疫苗后的突破感染(breakthrough infection)病例。这些病例与未接种疫苗的患者病毒载量无显著差异。
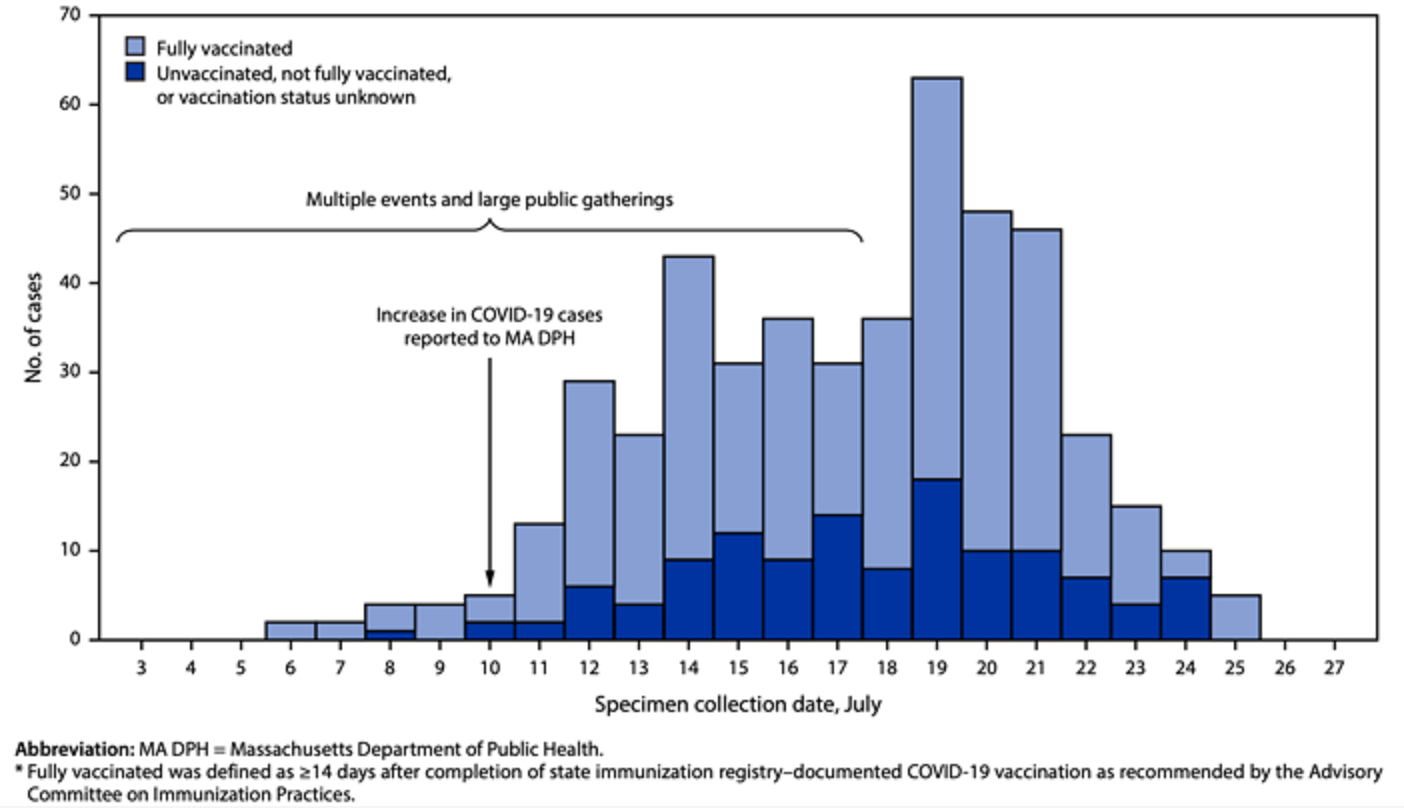
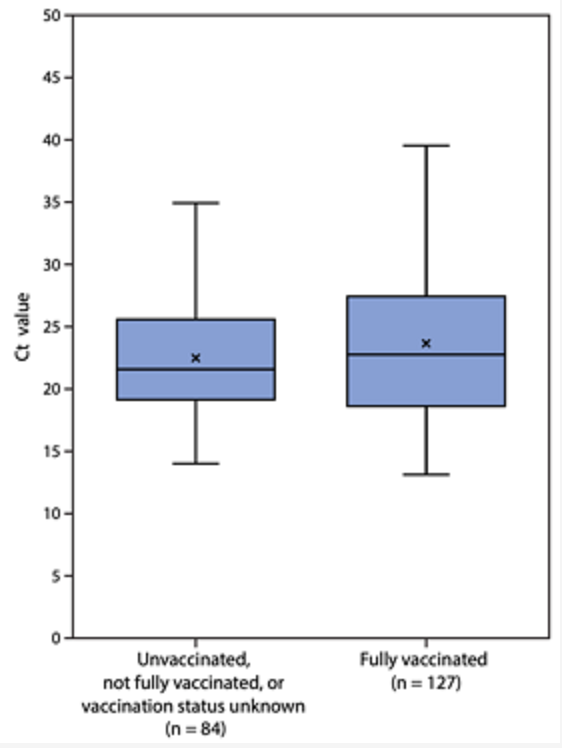
以色列纳入了1497名完成2剂疫苗接种的医务工作者,发现39名突破病例。
突破病例患者感染前抗体滴度低于未感染者,抗体滴度高的突破患者病毒载量低。
大部分突破病例无症状或者轻微症状,19%的突破病例症状持续时间超过6周。
但未发现包括病例家庭成员在内的二次传播。
第二部分:疫苗对新冠变异株研究的方法学评价
2021年7月22日世界卫生组织发布“针对SARS-CoV-2变异毒株的疫苗有效性评估的临时指南”。(注:本文中大量使用VE(指vaccine effectiveness)
目录:
1. 发布背景介绍
2. 对变异毒株的监测。
3. 疫苗对变异毒株有效性降低的早期触发因素。
3.1 疫苗的突破性病例和新的变异毒株
3.2 COVID-19流行病学的变化可能表明疫苗的减少对抗变异毒株的有效性。
3.3 使用突破性病例进行筛选的方法,以评估在变异毒株的情况下,疫苗有效性是否可能低于预期。
4. 仅依据病例的方法评估疫苗对变异毒株的有效性。
4.1 接种疫苗和未接种疫苗病例中变异毒株流行率的比较
4.2 筛分分析(解释:筛分分析(或级配测试)是土木工程和化学工程中使用的一种做法或程序,通过让材料通过一系列来评估颗粒材料的粒度分布(也称为级配)筛目尺寸逐渐变小的筛子,并称量每个筛子阻止的材料量作为整个质量的一部分)。
5. 对变异毒株进行全面的疫苗有效性评估。
5.1 当新的变异毒株共存时对COVID-19疫苗有效性的评价
A. 当大多数病例具有基因组特征时
B. 当大多数病例不具备基因组特征时
5.2 当变异毒株为主要流行毒株时COVID-19疫苗有效性的评价
6. 估计疫苗对变异毒株的有效性时,对基因测序的分析考虑
7. 对新变异毒株的疫苗有效性研究中的偏倚
1、发布的背景:
随着大流行病的发展,新的变种可能会随时出现,特别是在高发病率和低疫苗覆盖率的地区和群体。基因组和结构生物学研究、动物研究和体外中和试验可能表明,疫苗对某一特定变异毒株的保护作用可能较弱。然而,疫苗预防变异毒株感染和致病的有效性较低,最有力的证据是通过随机对照临床试验。但是,在对一种新疫苗进行随机对照试验时,突然出现一种新的变异毒株流行的情况十分罕见。新的突变毒株往往发生在疫苗临床试验完成后或疫苗试验地区以外。因此,大多数关于疫苗对新的突变株有效性的流行病学数据主要来自观察性研究。
鉴于以上情况,世卫组织发布了关于开展疫苗有效性评估最佳实践的临时指南。指南中的建议适用于对变异毒株进行疫苗有效性评估。然而,对变异毒株的疫苗有效性评估也可能会需要采取临时指南中没有描述的方法。
2、流行病学监测:
系统的流行病学监测必须与病毒的基因组特征相结合,以评估对变异毒株的抵抗力。世卫组织已经发布了关于COVID-19监测和病毒分离物的基因测序的临时指南。世卫组织正在发布关于SARS-CoV-2变异毒株监测的最新指南,其中强调在常规监测中增加基因测序,对病例进行基因测序采样,报告新的变异毒株,以及流行变异毒株对公共卫生和传播控制措施的影响。
监测要点:
a.常规监测样本进行基因组鉴定应该兼顾多种因素的抽样策略,抽样方法应该是系统的,对年龄组、地理分布和致病严重程度具有代表性;b.监测应该是连续且及时的,这样系统监测可以及早发现变异毒株,并可掌握它们在人群中的分布比例。c.收集将被测序的病例样本的基础数据十分重要,应包括日期和地点、患者特征、病例是输入的还是本土的、临床表现以及病例严重程度(若有)。d.此外还需要监测确诊病例的疫苗接种情况。对于突破性病例,应收集疫苗类型和接种日期,以评估是否可能发生疫苗免疫逃逸的情况。
3、新变异毒株的疫苗效力下降的早期预警(或触发)
3.1疫苗突破性病例和新变异毒株
无论何种病毒株,都会出现疫苗突破性病例,因为没有一种疫苗是100%有效的。突破性病例出现并不意味着一定是疫苗失败。然而,疫苗突破性病例可能预示着疫苗对新出现的病毒的有效性降低。无症状的突破性病例是指在完成所有推荐剂量的疫苗系列后≥14天,从无症状的COVID-19患者的呼吸道标本检测到SARS-CoV-2的RNA或抗原。有症状的突破性病例是指,在完成所有推荐剂量的疫苗系列后≥14天,从有有症状的COVID-19患者的呼吸道标本检测到SARS-CoV-2的RNA或抗原。由变异毒株引起的疫苗突破性病例的模式可能取决于个人对疫苗接种的免疫反应,如下文所述。
A.初始疫苗失败[保护性免疫反应不足]。由于未知的原因,一些疫苗接种可能完全不能在一部分接种者中引起保护性免疫反应。这种现象最常与活病毒疫苗有关,如麻疹,但任何疫苗都可能发生,无论是活疫苗还是灭活。初始疫苗失效还可能由于其他原因而发生;例如,由于冷链断裂、接种前疫苗受损、接种不当或受种者存在潜在的免疫缺陷。对于许多患有初始疫苗失败的人来说,其原因不明。无论一个人接触的是何种变异毒株,这种失败模式都适用,因为它取决于未能产生免疫反应。
B.疫苗改变致病情况。个体免疫反应可能无法预防感染或致病,但可能导致较少的症状或较轻的结果。个体免疫反应最初可能很强,足以预防任何感染或致病,但随着时间的推移可能会减弱,仅能在接种疫苗后某个时间预防重症的发生。然而,疫苗初始免疫反应较低的新变异毒株可能会在接种疫苗后更早地逃避对疫苗的免疫反应,导致接种疫苗后更早发生的突破性感染中致病的严重程度增加。
C."暴露阈值"疫苗。疫苗的有效性和疫苗突破性病例的发生频率可能因暴露水平的不同而不同。因此,对疫苗突破性病例的调查应包括背景、接触的密切程度、当地流行病学和其他可能影响个人或群体接触水平的环境因素。值得关注的变异毒株似乎更具传播性,部分原因是病毒载量和复制增加。此外,阻断某些新变异毒株(如Beta和Delta)所需的中和抗体的滴度更高。这些因素可能使新变异毒株在较低的暴露水平上引起突破性感染和/或致病;尽管这中情况很难衡量。
D.继发性疫苗失效。在疫苗因免疫力减弱而不再预防致病之前,接种疫苗可提供一段时间的保护。抗体浓度和细胞介导的免疫力的衰减可能在几个月到几年内发生,被感染的风险可能与前述的阈值有关。抗体浓度高于与保护相关的阈值,可能会预防感染或致病,而浓度低于阈值可能无法提供保护。从流行病学的角度来看,疫苗突破会在人群接种后的某个时间开始增加,这可能会在首批疫苗接种的人群中提前发生(如老年人、医护人员)。由于对新变异毒株的抗体中和作用可能较低,因此,与疫苗参考株相比,新变异毒株导致的保护性丧失和疫苗突破性病例可能会更早出现,尽管这一点还有待验证。值得注意的是,由于保护作用同时依赖于体液免疫和细胞免疫,较低的抗体水平不一定意味着免疫的整体水平,因为细胞免疫可能仍在提供保护,特别是预防重症。
3.2COVID-19的流行病学变化可能表明疫苗对新变异毒株的有效性降低
除了疫苗突破性病例的增加,COVID-19的流行病学变化可能提供了一个与疫苗效力下降有关的变异毒株流行的早期信号。在人群中达到较高的疫苗接种覆盖率后的几周内,可能会在目标群体中观察到致病发病率的大幅下降,正如在以色列快速推广疫苗时观察到的情况。下降趋势的意外减缓或逆转可能预示着对流行病毒的免疫力下降,特别是在新出现变异株的情况下。在疫苗接种率高的人群中,COVID-19住院人数或死亡人数的增加也可能是VE降低的信号,在疫苗接种率高的聚居社区,如长期护理设施或军营,致病的暴发也可能是这样。在所有这些情况下,基因测序应该是调查的一部分,以确定一个新的变异毒株是否在人群中变得更加普遍。
3.3使用突破性病例进行筛选方法,以评估在新变异毒株出现的情况下,疫苗有效性是否会低于预期。
仅仅评估突破性病例并不能量化VE,还需要人群疫苗接种覆盖率的数据。通过比较病例中的疫苗接种覆盖率和病例来源整体人群的疫苗覆盖率的筛选方法,可以估计疫苗对新变异毒株的VE。
该筛选方法可作为一种快速工具,用于评估疫苗的有效性是否符合预期,包括针对新变异毒株。当VE估计值低于临床试验或观察性研究,应开展更严格的VE评估。粗略估计的VE低于预期,可能是由于新变异毒株造成的。但也应调查其他潜在原因(见下BOX1)。
使用筛查方法计算粗略的VE只需要两个数据点:完全接种疫苗者发生的总病例的百分比(即突破性病例占所有病例的比例);以及人口中的疫苗接种率。因此,筛查方法相对容易执行且费用低廉。图1显示了接种疫苗的病例比例、接种疫苗的来源人口比例和粗略的VE之间的关系。如果有变异毒株感染的病例数据,可以用筛查法计算出变异毒株的粗VE,即用接种疫苗的所有病例的百分比代替接种疫苗变异毒株病例的百分比。
BOX1. 有效性(VE)粗略估计不同于预期的可能原因

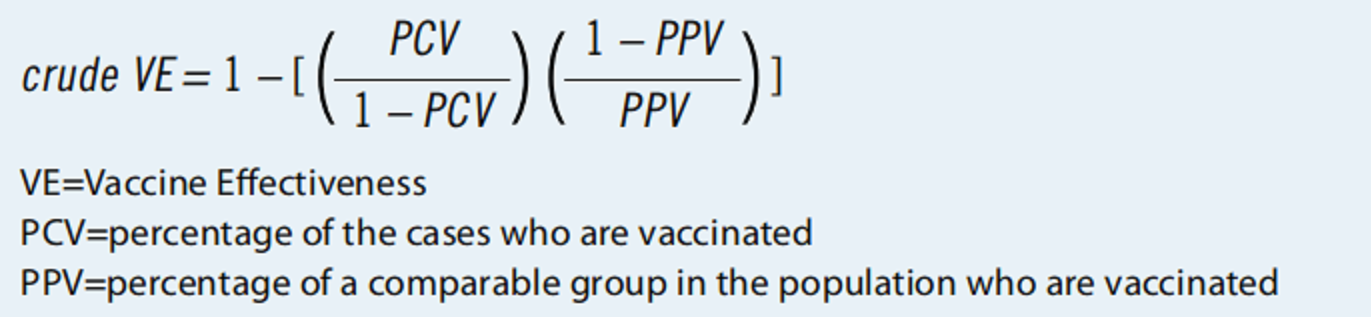
图1.筛选方法:接种人口百分比(PPV)、估计的疫苗效力和接种病例百分比(PCV)之间的关系
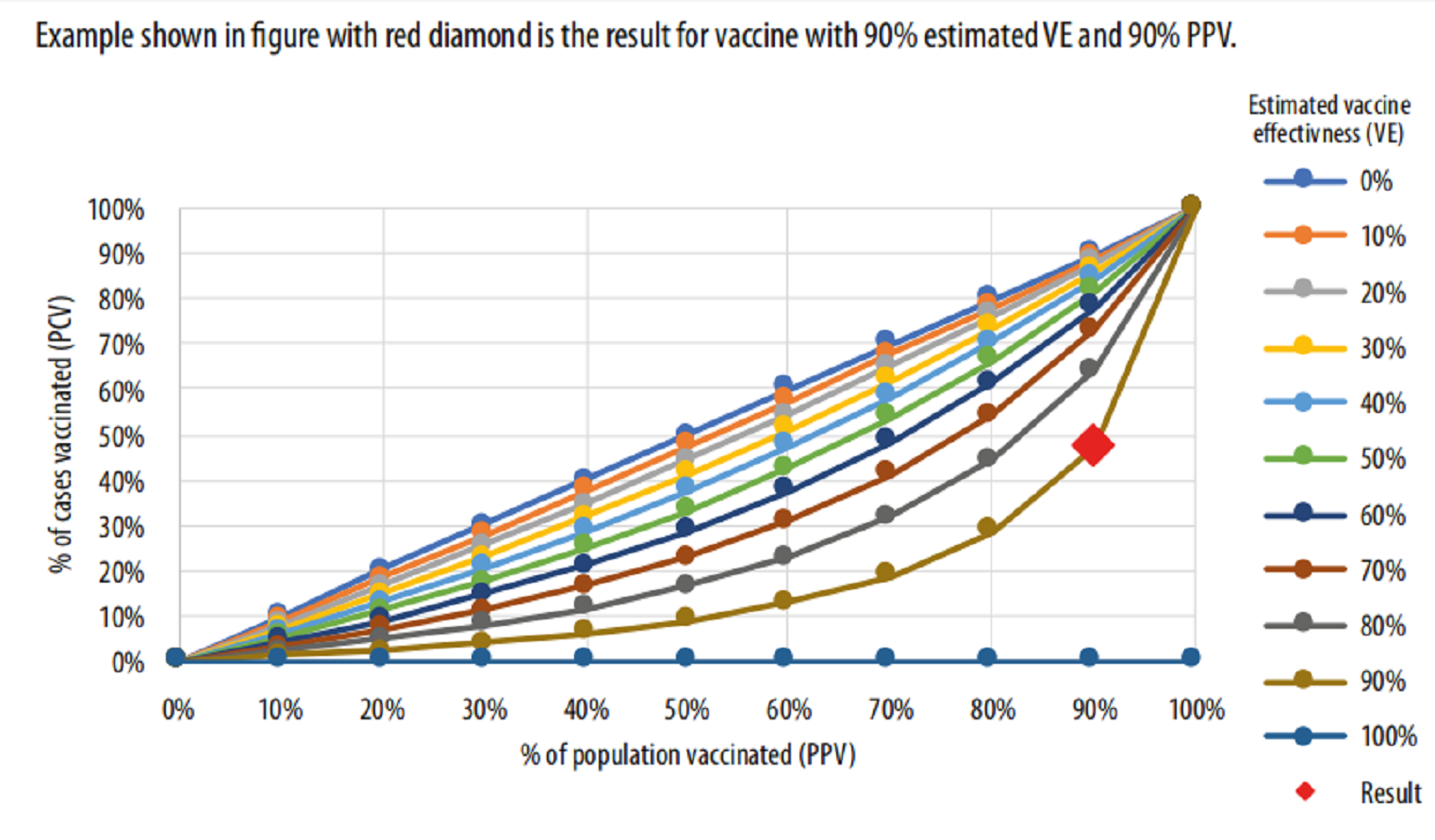
接种疫苗的病例比例(公式中的PCV)可以从国家或地区,甚至可以从一个或几个医疗机构(如哨点)的监测数据中获得。这些数据应以病例为基础,以便于按疫苗目标群体和疫苗类型进行分层。至少评价的病例在发病时必须有接种疫苗的资格(例如,在有疫苗时成为接种目标),病例数据应包括症状(或无症状感染)、严重程度(住院、严重疾病或死亡)、发病日期、疫苗品牌、接受疫苗剂量(多少剂)以及接种最后一剂的日期。此外,如果有条件还应包括通过基因测序确定的变异毒株类型。
在根据监测病例数据计算接种疫苗的病例百分比(PCV)时,我们建议如下:
只有符合接种条件的病例才应包括在PCV的计算中(例如,目标年龄组)。 只有实验室确诊的病例才应包括在内。 只有在部分人群接受了全部推荐的疫苗接种后发生的病例疫苗的时间安排(如2个剂量的mRNA疫苗)应包括在内。 如果症状发生在完成规定疫苗剂量的接种后1-2周,则应视为完全接种。应排除那些在症状出现前至少1-2周没有完成推荐的疫苗接种计划的病例。 如果对足够数量的病例进行基因组鉴定(如测序、SNP检测),病例可以被分层为疫苗参考病毒或变异毒株。然而,必须考虑测序算法,以确保在被评估的人群中随机进行(见6.估计变异毒株疫苗有效性时对基因测序的分析考虑)。 疫苗接种数据应包括疫苗类型或品牌。 最小样本量将由疫苗覆盖率决定。病例的样本量为如下表1所示,把握度为80%。 结果可以按接种目标群体(如年龄组)和时间(如周或月)进行分层,就像对流感疫苗评估那样。
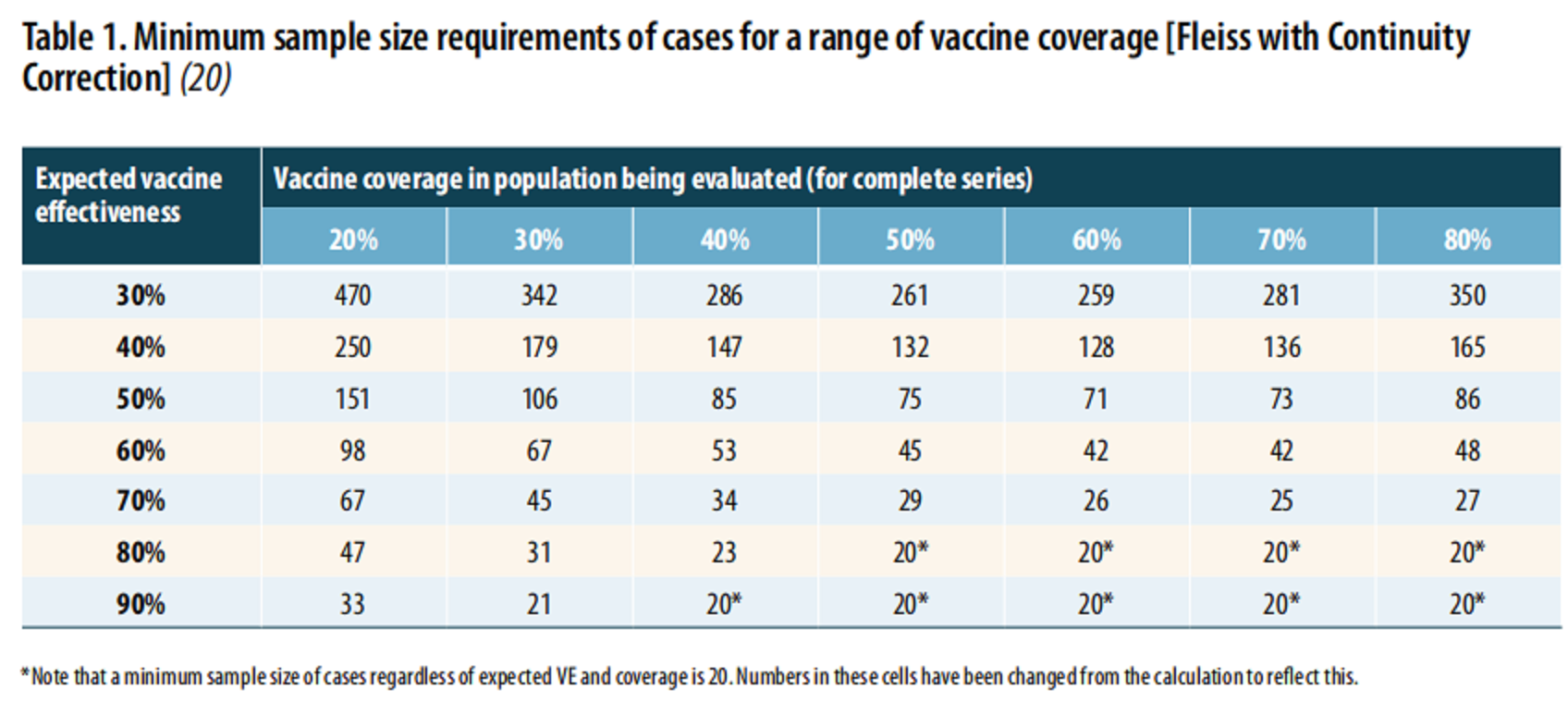
疫苗接种群体(公式中的PPV)中某一可比群体接种疫苗的百分比可以从行政数据库、疫苗接种登记处或覆盖率调查中获得。覆盖率数据的关键标准见下文:
覆盖率数据应该是基于相同的人群(如城市、地区)和相同的研究目标人群,而且目标人群中已经识别出感染的病例。 人口覆盖率只应在符合疫苗接种条件的人群中进行,并以相同的方式进行分层。病例数据的分层方式(例如,按年龄组、按疫苗类型或产品和按日期)。 应计算完整的疫苗接种系列的覆盖率,即来源的人群充分接种疫苗的百分比。 对于疫苗类型或特定产品的VE,来源人群应排除已接种其他类型或品牌疫苗的人群。 时间考虑 - 在计算PPV时,应使用病例发病前1-2周在来源人口中的疫苗接种率,以便有足够的时间达到完全免疫。 - 对于按月汇总的病例,可以使用前一个月的中点时间的疫苗接种率。 - 如果结局是住院或重症,则可使用住院、重症或死亡前3-4周的疫苗接种覆盖率来计算从发病到这些更严重结局的时间。
将上述计算结果与PPV和PCV一起纳入,以计算出粗略的VE。95%的置信区间(CI)可以通过使用Farrington等所述的逻辑回归来计算。
该筛查方法有几个局限性。粗略的VE估计值没有根据个人特征或其他诱因(如合并症)进行充分调整。与监测有关的偏倚(如谁被检测、数据缺失)可能影响结果。通常情况下,筛查方法适用于具有稳定的疫苗接种覆盖率的地方性致病,而且疫苗接种不会产生高水平的群体免疫力。对于COVID-19,这些属性中的一些是未知的或可能不适用。最后,监测和覆盖率数据的质量不佳,不包括产生病例的同一人群,会导致粗略的VE估计值出现巨大差异。
4、基于病例评估疫苗对新变异毒株有效性
4.1接种疫苗和未接种疫苗病例中变异毒株流行率的比较
在流行中发现多个SARS-CoV-2变异毒株的情况下,对病例的分析可以提供疫苗对变异毒株有效性下降的早期预警信号。其中一项分析完全依靠监测数据,是对变异毒株感染病例中的疫苗接种与参考毒株感染的病例中的疫苗接种率进行比较。尽管没有提供VE的估计值,但仅对病例的分析表明,相对于对疫苗参考毒株的保护,对变异毒株的保护是否下降。如果对特定变种的保护效果较差,那么在特定的时间和地点,变异毒株引起的疫苗突破性病例的发生率就会增加。
所有纳入单例分析的COVID-19病例都必须进行基因组鉴定。为了增加样本量,SNP检测法可用于变异株动态特征良好的情况下(例如,L452R阳性SNP检测试验可能表明是Delta,或者N501Y+E484K检测阳性可能表明是Beta和/或Gamma,如果没有其他流行变异毒株携带该突变或突变组合)。参考病毒可能是那些在疫苗生产中使用的病毒,或者是疫苗已经证明有效的病毒,包括在许多国家已经占主导地位的Alpha变异毒株。由参考SARS-CoV-2病毒感染的病例和仅对病例进行分析变异毒株必须在同一来源人群和同一时间段内确定,以控制疫苗接种率和变异毒株发病率的变化。
可以建立一个简单的2×2表格进行个案分析,具体如下
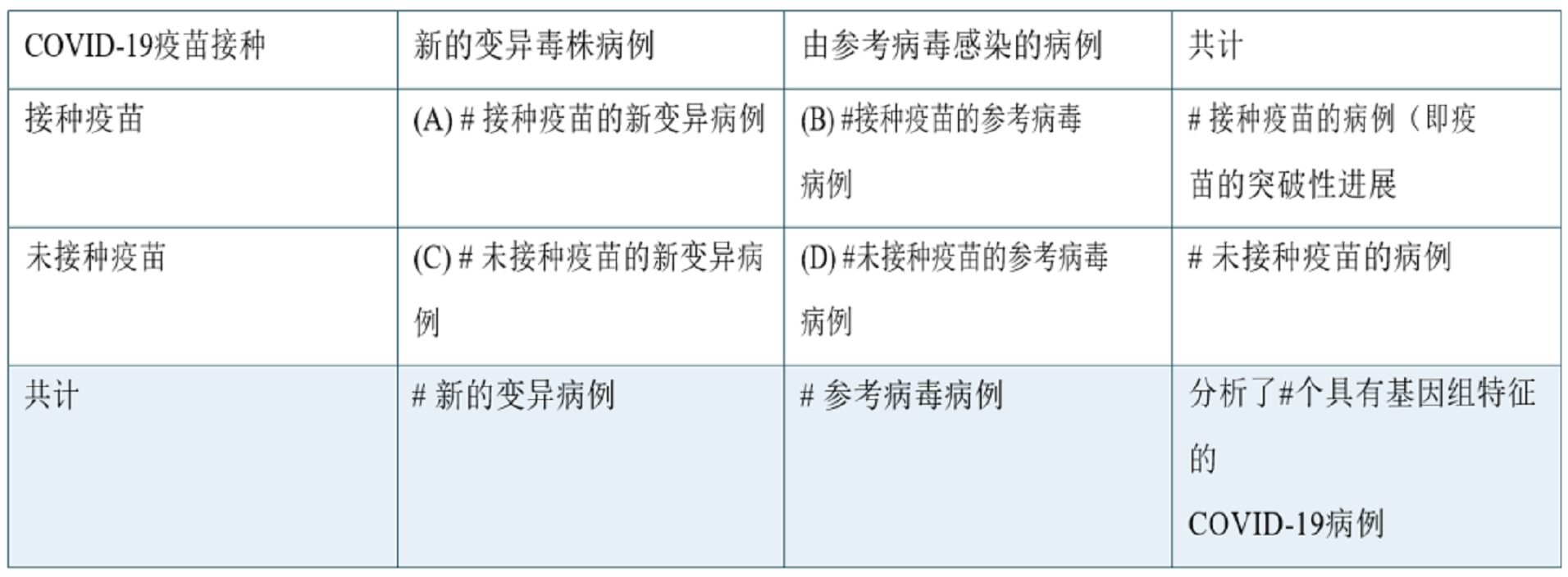
粗略的比值比(OR)是指新变异病例(A/C)中接种疫苗的比值比除以参考病毒病例(B/D)中接种疫苗的比值比,或(A*D)/(B*C)。当新变异病例中接种疫苗的比值比高于参考病毒病例中接种疫苗的比值比时,OR>1。当OR大于1时,表明与对参考病毒感染的病例的有效性相比,对新变异株的疫苗有效性降低(27)。对于更高级的分析,可以通过回归模型,通常是Logistic或对数二项式模型,独立考虑每个新变异株来调整混杂因素。
需要注意的是,仅有病例的分析并不能绝对的估计准确疫苗有效性。虽然它类似于估计肺炎球菌疫苗接种效果的间接队列分析,但间接队列方法假设疫苗对非疫苗型的风险没有影响的前体。
相当于假设COVID-19疫苗对新变种没有保护作用,但情况可能并非如此,因为根据现有的免疫学和有效性数据,到目前为止,COVID-19疫苗似乎对新变种有一定的有效性。因此,仅有病例的分析只能表明,与参考病毒相比,疫苗对新变种的VE是否有相对下降。
为了调整新变异株流行时间和按年龄指征的疫苗推广的潜在混杂因素,在仅有病例的分析中应按日期进行分层(若不按入组时间匹配情况下)。此外,可以通过发病时间和潜在的混杂因素(如年龄和居住地),将变异毒株感染的病例与疫苗参考病毒感染的病例进行匹配,并使用精确检验(如McNemar's)或条件逻辑回归,作为匹配分析来估计疫苗接种比值比。最后,如前所述,在出现后数周内的快速替代意味着采取仅有病例的方法的时间窗口可能很短,由于参考毒株导致的病例迅速减少到不可能再进行比较的水平。
4.2筛分分析
筛分分析可以作为一种聚焦于COVID-19疫苗对特定的变异株系(即VOIs/VOCs)VE下降的替代方法。筛分分析与上述的个案分析有关,即比较来自接种疫苗和未接种疫苗病例的基因组序列。这种方法使用系统发育学、生物信息学和统计学方法,不需要对基因组序列中的哪些变化有强烈的先验假设(例如,不需要对病例进行先验挑选)。虽然筛分分析最初是为了评估疫苗和安慰剂接受者的疫苗疗效试验中的病毒遗传特征,但这种方法也可以应用于调查疫苗在人群中推广后导致VE下降的病毒学关键因素。这些决定因素可以在目前正在流行的病毒变异株中识别出,或者预测未来哪些变异株可能更有可能逃避疫苗免疫反应。
如果只有一个变异株替代了几乎所有的序列,或者有多个变异株共同流行,则可以在不同的环境中使用筛分分析。例如,Alpha代表了几种环境中的大多数感染,因此可能排除了Alpha与其他病毒的分析。然而,Alpha有一些具有特定突变的亚系,筛分方法可以识别与VE降低有关的亚系或特定突变。根据分析的重点,筛分分析方法可分为三类(详见指南)。
与其他分析一样,筛分分析需要控制时间、地点和人口因素的混杂,应与熟悉这种复杂方法的统计学家协商进行。
5、对新的突变毒株进行疫苗有效性的全面评估
如果COVID-19流行病学的变化、对突破性病例的检查或仅对病例的分析表明,对新变异毒株的VE可能降低,那么可能需要进行全面的VE评估。对新变异毒株进行VE评估的方法可以考虑在两种情况下进行:a)当以前占优势变异毒株与新变异毒株共同流行时;b)当新变异毒株成为人群中占优势的毒株时。
用于估计COVID-19疫苗对任何SARS-CoV-2病毒所致致病或感染的有效性的检测阴性设计病例对照研究(TND)也可用于估计COVID-19对变异毒株的VE。这种方法与流感疫苗的特异性VE评估相似。在这项分析中,将变异毒株导致的病例中的COVID-19疫苗接种情况(或接种比值)与SARS-CoV-2检测阴性者的疫苗接种情况进行比较。这种TND设计中,针对新变异毒株感染的病例的VE提供了针对特定结果(如致病、感染)的绝对而非相对的VE估计。
估算VE的样本量估计必须针对每个变异毒株和疫苗类型分别计算,可以使用之前如临时指南中所述引用的样本量公式/计算器。针对变异毒株的VE分析是在与COVID-19检测阴性对比组相同时间段内的相同来源人群的数据上进行的,以控制疫苗接种率的变化。
如同在只有一个变异毒株流行的病例对照研究分析中一样,在有多个变异毒株流行的情况下,每个变异毒株的比值比(OR)是每个变异毒株的病例中接种疫苗的比值(即#接种疫苗/#未接种疫苗)除以检测阴性对照中接种疫苗的比值。疫苗的有效性被估计为每个变异毒株的(1-OR)×100。请注意,用于分析COVID-19VE对新变异毒株的检测阴性对照组将是每个变异毒株的同一组。
可以从2×2的表格中计算出比值,或通过逻辑回归来调整潜在的混杂因素。一个用于估计参考病毒和新变异毒株的VE的简单表格可以设置如下:
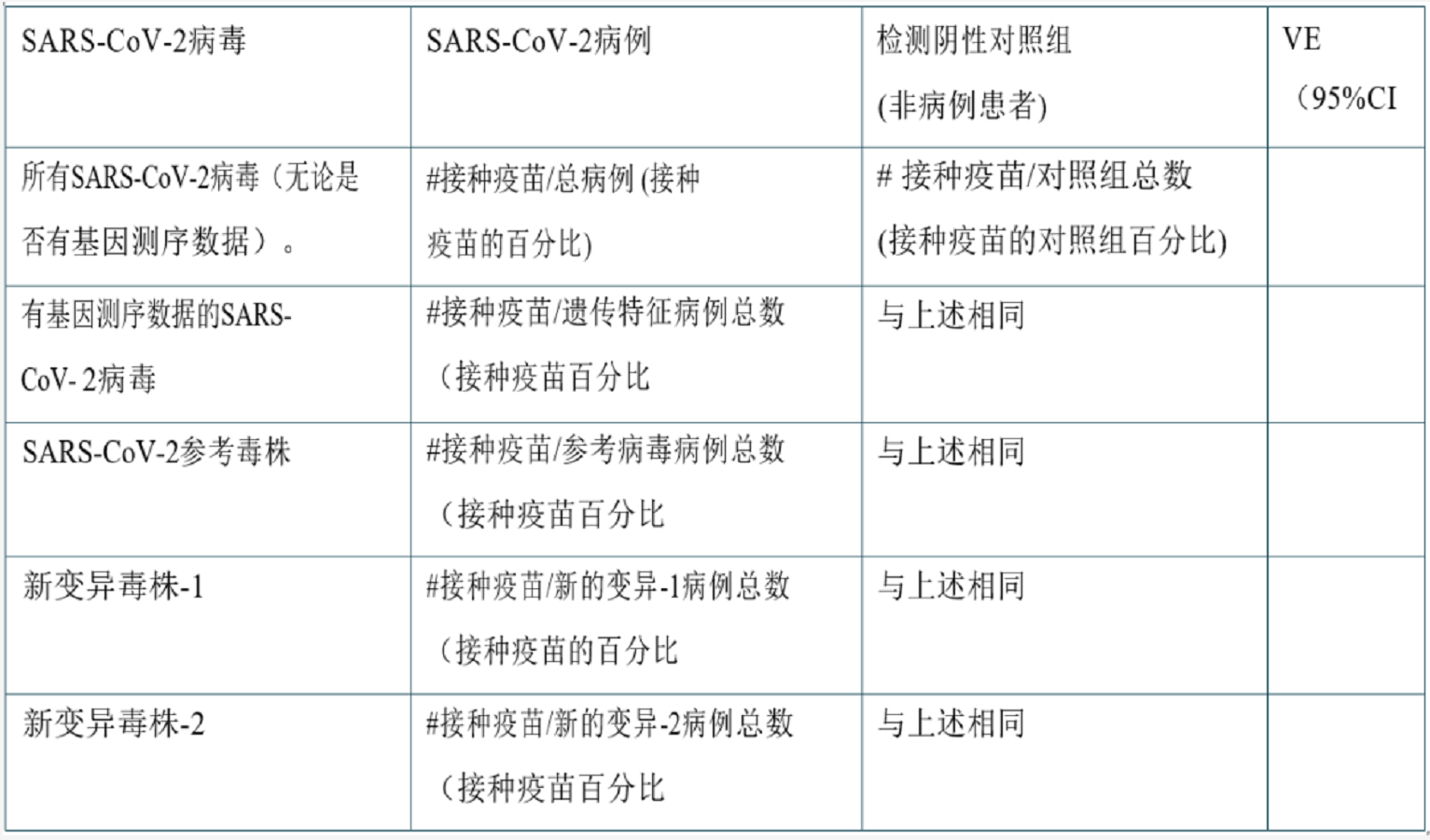
如果与参考病毒相比,一个新变异毒株的VE较低,说明针对该变异毒株的VE降低了(特别是在95%的置信区间不重叠的情况下)。如果针对所有SARS-CoV-2病毒的VE(无论是否进行了基因组鉴定)与所有基因测序鉴定的SARS-CoV-2病毒的VE不同,这说明在选择测序的病毒时可能存在偏倚。
当大多数病例缺乏病毒基因组数据时
对新变异毒株进行VE评估的金标准需要对研究人群中的所有病例进行基因组特征分析。世卫组织鼓励在进行VE评估时尽可能完整地描述基因组特征。然而,在大多数情况下,VE研究中的大多数COVID-19病例将无法获得基因组特征分析。只有一部分病例会有基因组特征,或者流行变异毒株的分布会从人口层面的抽样中得出。在这些情况下,针对新变异毒株的VE可能只能从VE评估中推断出来。新变异毒株对VE评估中发现的总体VE的贡献将取决于它在人群中的流行率--流行率越高,对总体VE的贡献越大。然而,如前所述,在有新变异毒株流行的人群中,VE低于预期,除了针对该变异毒株的VE较低外,还有许多其他原因。(见BOX1)
基于无基因测序(或替代物,如Alpha或SNP检测突变的S基因靶点失败)的VE研究,推断疫苗对新变异毒株的VE具有挑战性,应结合研究人群中新变异毒株的流行率来解释,并考虑到发现与预期不同的VE的其他原因。
5.2当变异毒株成为主要流行毒株时
如果有代表性的基因测序数据证明一个新的变异毒株已经完全取代了以前的病毒株,那么进行疫苗有效性研究的最佳实践方法可参见《COVID-19疫苗有效性评估临时指南》。事先确定感兴趣的研究结局,如感染、有症状的致病或重症。多种研究设计,如队列、传统的和检测阴性的病例对照研究,都可用于评估新变异毒株的VE。仍然建议对实验室确认的结局而不是基于症状的结局进行评估,并使用研究者记录的而不是患者自我报告的疫苗接种数据。应收集的协变量和结果报告指南可参见上述指南。
在使用这些相同的方法来评估新变异毒株时,可能会出现一些独特的困难。如果变异毒株在疫苗推广时已经占主导地位,那么这些方法就基本没有变化。然而,如果变异毒株在疫苗引进后的某个时间点完全取代了以前的毒株,那么在评估变种的时候,该国的疫苗推广工作将处于更高级的阶段。在这种情况下,人口中未接种疫苗的人就会减少。在覆盖率达到90%之前进行VE研究是明智的,因为剩下的未接种者可能会有非典型的感染风险,这可能会导致VE的估计出现偏倚。队列和病例对照研究都可能受到影响。此外,在高度接种的人群中,检测方法可能已经与疫苗推广初期的情况发生了变化。在对变异毒株进行VE研究时,应评估当时的检测方法,以评估可能的偏倚;这对TND来说可能特别重要。如果在新变异毒株成为主导的时候,人们已经接种了相当长的时间,那么疫苗诱导的免疫保护对所有SARS-CoV-2毒株都可能减弱。这种减弱可能会被误解为对变异毒株的VE较低。最后,用于识别新变异毒株的实验室测试应该对目前流行变异毒株达到推荐的≥85%的灵敏度和≥98%的特异性,尽管在进行VE研究时可能还不知道。对新变异毒株较低的测试性能会导致错误的分类,特别是在TND中。对于未来的新变异毒株,可能需要对目前使用的RT-PCR测试进行调整。
6、在估计疫苗VE对新毒株有效性时基因测序分析的考量
对于VE研究中的基因测序,还应该考虑几个问题。被测序的病毒应该在VE研究人群的具有SARS-CoV-2病毒的代表性。选择哪些病毒进行测序应与疫苗接种状态、病例人口统计学或临床结果无关。
重要的是要从按日期和入院地点/来源人群(如住院病人与门诊病人)相匹配的病例中收集病毒标本。在VE研究中,可以通过几种方式取样:(1)所有病例(在那些样本在技术上可行的情况下,如具有足够的病毒浓度);(2)在预先设定的时间范围内随机选择病例;(3)根据病例总数和实验室能力,系统地随机取样,如每4个病例;(4)每天或每周取第一个固定数量的病例(如5或10),按地点和年龄分层。无论采用哪种方法,都应确保每种病毒有相同的抽样概率。由于抽样框架可能因方法不同而不同,我们建议咨询统计学家,以便在分析数据时对抽样分数进行调整。
由于非代表性的抽样,一些偏倚可能会影响VE的解释。例如,接种疫苗的人可能比未接种疫苗的人有较低的病毒载量。Ct值>30的病毒通常更难测序。这意味着,与未接种疫苗的人相比,接种疫苗的人的样本中可能有较低比例的病毒可以被测序。如果病毒载量也因新变异毒株而变化,这可能会造成混杂和有偏倚的VE估计。为了检查与测序样本有关的潜在偏倚,可以采取不同的方法。(1)比较总体VE和仅来自测序病例的VE。(2)将有测序病毒的病例与没有测序病毒的病例以及检测阴性的对照组的人口统计学、地区分布和日期进行比较。
如前所述,如果没有对VE研究受试者病毒进行测序,那么在研究之外获得的同期测序信息可以帮助根据人群中流行的新变异毒株来解释VE结果。然而,可获得测序数据的人群可能与VE研究人群不同,而且选择测序样本的标准可能不是随机的(如针对更多的疫苗接种者,针对特定的临床状况),从而导致对VE对新变异毒株的错误结论。
7、变异毒株的疫苗有效性研究中的偏倚
在估计总体VE时任何偏倚都可能出现,在分别估计某一特定毒株(包括变异毒株)的VE时也可能出现。例如,如果接种疫苗与接触COVID-19呈正相关(例如,由于职业原因,如医护人员),那么,如果在分析中不对这种接触进行调整,则估计的整体VE和每个毒株的VE都可能比真实的VE有所偏低。如果医护人员与其他人接触变异毒株的比例相同,那么在比较不同变种病例的疫苗状况时,相对VE应该是无偏倚的。同样,《临时指南》表3中列出的许多其他潜在偏倚--如果它们同样适用于所有变异毒株--可能会使绝对VE估计值出现偏倚,但不会使相对VE估计值出现显著偏倚。
对新变异毒株的感染或致病的相对VE的分析中可能出现一些不同形式的偏倚。如果一种新变异毒株可能导致严重疾病,那么出现于严重疾病的偏倚也将影响疫苗对该新变异毒株(如Covid-19试验的假阴性)的VE估计。其他更复杂的相互作用可能会发生,导致在估计不同变异毒株的VE时出现不同的偏倚,从而导致有偏倚的比较性的VE估计。例如,接种疫苗后免疫力随着时间的推移而减弱的情况,如果人口中新变异毒株的频率与以前占主导地位的毒株相比随着时间的推移而增加,那么在感染时间和被变异毒株感染的机会之间就会有一个正相关。如果发生了真正的有效性减弱或由于易感个体的耗尽而导致的虚假减弱,这将导致对新变异毒株的VE估计错误地低于以前的主要流行毒株,因此在比较性VE估计中可能会低估新变异毒株的VE。不过,这个问题可以通过在日期上进行匹配比较来解决。
如果对新变异毒株的诊断灵敏度较低,这可能会或可能不会导致对相对VE的估计出现偏倚,这取决于灵敏度较低是否是针对接种者的。如前所述,接种者的病毒载量较低,加上PCR扩增的不理想,可以高估疫苗对新变异毒株更有效性,因为在接种者和感染者身上看不到PCR扩增信号。如果较低的敏感性与疫苗状态无关,这会使绝对的VE估计值出现偏倚。
需要进行更多的研究,以更好地了解可能出现的偏倚,这些偏倚可能是由于过去感染不同毒株的不同保护水平、不同毒株的不同VE以及感染后和疫苗衍生的免疫力的未知保护时间的组合。
结论
随着COVID-19大流行的发展,新的SARS-CoV-2变种可能会继续出现。评估疫苗对这些变异毒株的表现至关重要,以便为免疫接种计划、政策制定者和疫苗开发者提供信息。本增编更新了世卫组织关于在出现新变异毒株的情况下对COVID-19疫苗进行VE研究的临时指南。
作者简介 邹晓辉 医学博士,中日友好医院临床感染实验室,中日医院呼吸中心,助理研究员。芝加哥大学计算机学院,美国阿岗国家实验室计算、环境、生命科学研究所(CELS)postdoc访问学者。国际流感和其他呼吸道病毒协会会员(Member),多本SCI杂志审稿人。主持国家自然科学基金(青年项目)1项,参入国家重点研发计划,国家科技重大专项多项。主要研究呼吸感染,临床宏基因组学病原检测,重症病毒感染机制,基因组数据机器学习。发表SCI文章多篇。 王业明 医学博士,住院医师。主要研究方向为呼吸系统感染性疾病的临床研究。曾参与科技部H7N9应急专项、艾滋病和病毒性肝炎等重大传染病防治,比尔盖茨基金项目;以第一或共一作者发表SCI论著10余篇;clinical tiral杂志中文版编委。 END 作者|邹晓辉、王业明 审校|陈宏斌、余方友




